SISTEMA ENDOCRINO
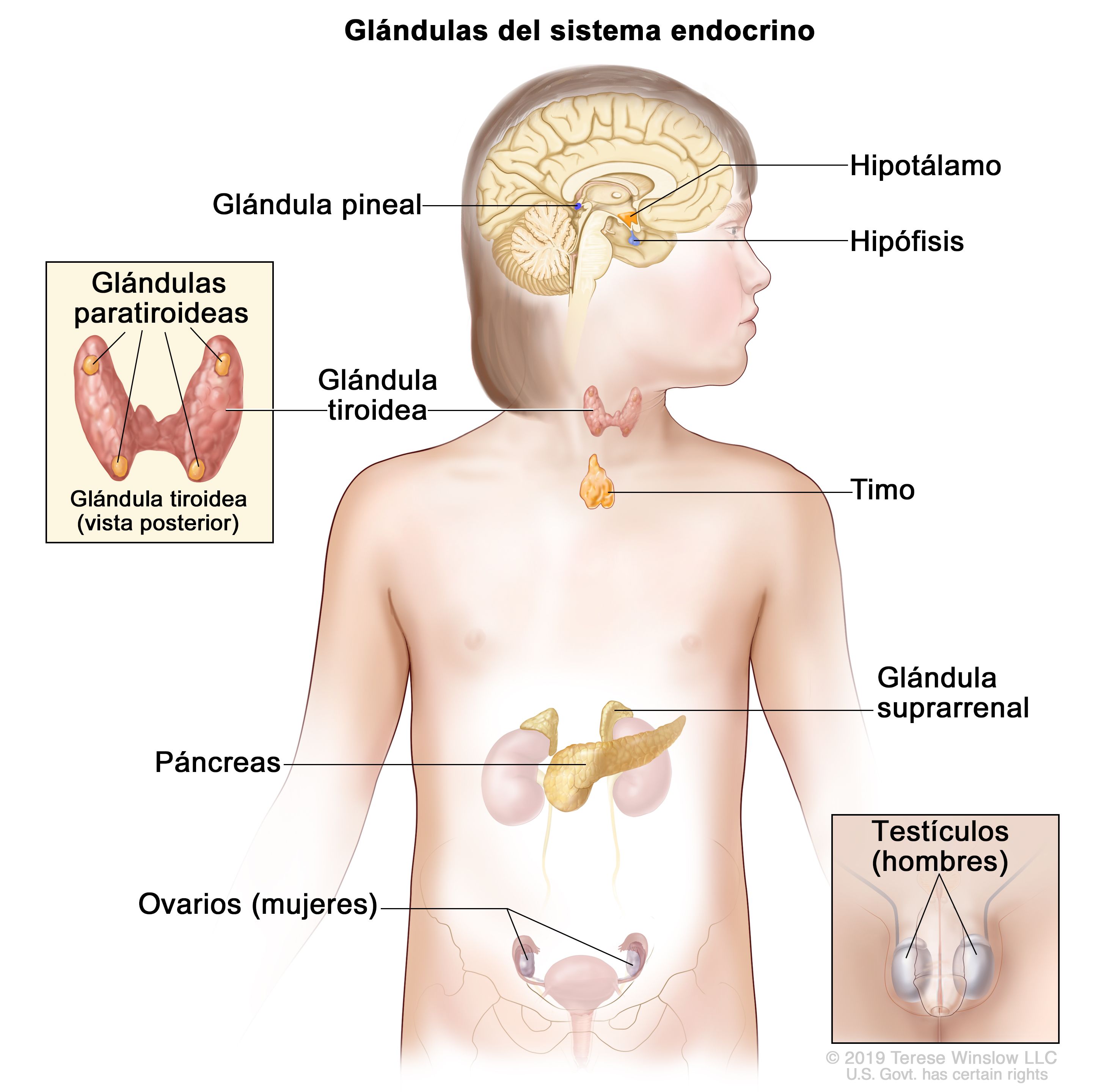
Glándulas y órganos del sistema endocrino. El sistema endocrino produce hormonas que controlan muchas funciones importantes del cuerpo. Se compone de glándulas y órganos como los siguientes: el hipotálamo, la hipófisis, la glándula pineal, la glándula tiroidea, las glándulas paratiroideas, el timo, las glándulas suprarrenales, el páncreas y los órganos reproductores (ovarios en las mujeres y testículos en los hombres).
Tomado de Instituto Nacional del Cáncer (S.F):
https://www.cancer.gov/espanol/publicaciones/diccionarios/diccionario-cancer/def/sistema-endocrino
Suscribirse a:
Entradas (Atom)